Termodinâmica é um importante ramo da física. Podemos dizer com segurança que suas conquistas levaram ao surgimento da era tecnológica e determinaram em grande parte o curso da história humana nos últimos 300 anos. O artigo discute a primeira, segunda e terceira leis da termodinâmica e sua aplicação na prática.
O que é termodinâmica?
Antes de formular as leis da termodinâmica, vamos descobrir o que esta seção da física faz.
A palavra "termodinâmica" é de origem grega e significa "movimento devido ao calor". Ou seja, este ramo da física está envolvido no estudo de quaisquer processos, como resultado do qual a energia térmica é convertida em movimento mecânico e vice-versa.
As leis básicas da termodinâmica foram formuladas em meados do século XIX. A ciência do "movimento e calor" considera o comportamento de todo o sistema como um todo, estudando a mudança em seus parâmetros macroscópicos - temperatura, pressão e volume, e não prestando atenção à sua estrutura microscópica. Além disso, o primeiro deles desempenha um papel fundamental na formulação de leistermodinâmica na física. É curioso notar que eles são derivados apenas de observações experimentais.
O conceito de um sistema termodinâmico

Significa qualquer grupo de átomos, moléculas ou outros elementos que são considerados como um todo. Todas as três leis são formuladas para o chamado sistema termodinâmico. Exemplos são: a atmosfera da Terra, qualquer organismo vivo, a mistura de gases em um motor de combustão interna, etc.
Todos os sistemas em termodinâmica pertencem a um dos três tipos:
- Aberto. Eles trocam calor e matéria com o meio ambiente. Por exemplo, se a comida é cozida em uma panela em fogo aberto, este é um exemplo vívido de um sistema aberto, pois a panela recebe energia do ambiente externo (fogo), enquanto ela própria irradia energia na forma de calor, e a água também evapora dele (metabolismo).
- Fechado. Em tais sistemas não há troca de matéria com o ambiente, embora ocorra a troca de energia. Voltando ao caso anterior: se você cobrir a chaleira com uma tampa, poderá obter um sistema fechado.
- Isolado. Este é um tipo de sistema termodinâmico que não troca matéria ou energia com o espaço circundante. Um exemplo seria uma garrafa térmica contendo chá quente.
Temperatura termodinâmica

Este conceito significa a energia cinética das partículas que formam os corpos circundantes, que reflete a velocidademovimento aleatório de partículas. Quanto maior, maior a temperatura. Assim, reduzindo a energia cinética do sistema, nós o resfriamos.
Este conceito significa a energia cinética das partículas que formam os corpos circundantes, que reflete a velocidade do movimento caótico das partículas. Quanto maior, maior a temperatura. Assim, reduzindo a energia cinética do sistema, nós o resfriamos.
A temperatura termodinâmica é expressa em SI (Sistema Internacional de Unidades) em Kelvin (em homenagem ao cientista britânico William Kelvin, que primeiro propôs esta escala). Compreender a primeira, segunda e terceira leis da termodinâmica é impossível sem uma definição de temperatura.
Uma divisão de um grau na escala Kelvin também corresponde a um grau Celsius. A conversão entre essas unidades é realizada de acordo com a fórmula: TK =TC + 273, 15, onde TK e TC - temperaturas em kelvins e graus Celsius, respectivamente.
A peculiaridade da escala Kelvin é que ela não possui valores negativos. Zero nele (TC=-273, 15 oC) corresponde ao estado em que o movimento térmico das partículas do sistema está completamente ausente, eles parecem estar "congelados".
Conservação de energia e a 1ª lei da termodinâmica

Em 1824, Nicolas Léonard Sadi Carnot, engenheiro e físico francês, fez uma sugestão ousada que não apenas levou ao desenvolvimento da física, mas também se tornou um passo importante no aprimoramento da tecnologia. Delepode ser formulado da seguinte forma: "A energia não pode ser criada ou destruída, ela só pode ser transferida de um estado para outro."
De fato, a frase de Sadi Carnot postula a lei da conservação da energia, que formou a base da 1ª lei da termodinâmica: "Sempre que um sistema recebe energia do exterior, ele a converte em outras formas, a principal das que são térmicas e mecânicas."
A fórmula matemática da 1ª lei é escrita da seguinte forma:
Q=ΔU + A, aqui Q é a quantidade de calor transferida pelo ambiente para o sistema, ΔU é a variação da energia interna desse sistema, A é o trabalho mecânico perfeito.
Processos adiabáticos
Um bom exemplo é o movimento das massas de ar ao longo das encostas das montanhas. Essas massas são enormes (quilômetros ou mais), e o ar é um excelente isolante térmico. As propriedades observadas nos permitem considerar como adiabáticos quaisquer processos com massas de ar que ocorram em um curto espaço de tempo. Quando o ar sobe a encosta de uma montanha, sua pressão cai, ele se expande, ou seja, realiza trabalho mecânico e, como resultado, esfria. Ao contrário, o movimento descendente da massa de ar é acompanhado por um aumento de pressão nela, ela comprime e, devido a isso, fica muito quente.
A aplicação da lei da termodinâmica, que foi discutida no subtítulo anterior, é mais facilmente demonstrada usando o exemplo de um processo adiabático.
De acordo com a definição, como resultado não há troca de energia comambiente, ou seja, na equação acima, Q=0. Isso leva à seguinte expressão: ΔU=-A. O sinal de menos aqui significa que o sistema realiza trabalho mecânico reduzindo sua própria energia interna. Vale lembrar que a energia interna depende diretamente da temperatura do sistema.
Direção dos processos térmicos
Esta edição trata da 2ª lei da termodinâmica. Certamente todos notaram que, se você colocar dois objetos com temperaturas diferentes em contato, o frio sempre aquecerá e o quente esfriará. Observe que o processo inverso pode ocorrer dentro da estrutura da primeira lei da termodinâmica, mas nunca é implementado na prática.
A razão da irreversibilidade deste processo (e de todos os processos conhecidos no Universo) é a transição do sistema para um estado mais provável. No exemplo considerado com o contato de dois corpos de temperaturas diferentes, o estado mais provável será aquele em que todas as partículas do sistema terão a mesma energia cinética.
A segunda lei da termodinâmica pode ser formulada da seguinte forma: "O calor nunca pode ser transferido espontaneamente de um corpo frio para um quente." Se introduzirmos o conceito de entropia como uma medida de desordem, então ela pode ser representada da seguinte forma: "Qualquer processo termodinâmico prossegue com um aumento na entropia".
Motor térmico

Este termo é entendido como um sistema que, devido ao fornecimento de energia externa a ele, pode realizar trabalho mecânico. Primeiroas máquinas térmicas eram máquinas a vapor e foram inventadas no final do século XVII.
A segunda lei da termodinâmica desempenha um papel decisivo na determinação de sua eficácia. Sadi Carnot também estabeleceu que a eficiência máxima deste dispositivo é: Eficiência=(T2 - T1)/T2, aqui T2 e T1 são as temperaturas do aquecedor e do refrigerador. O trabalho mecânico só pode ser feito quando há um fluxo de calor de um corpo quente para um frio, e esse fluxo não pode ser 100% convertido em energia útil.
A figura abaixo mostra o princípio de funcionamento de uma máquina térmica (Qabs - calor transferido para a máquina, Qced - perda de calor, W - trabalho útil, P e V - pressão e volume de gás no pistão).
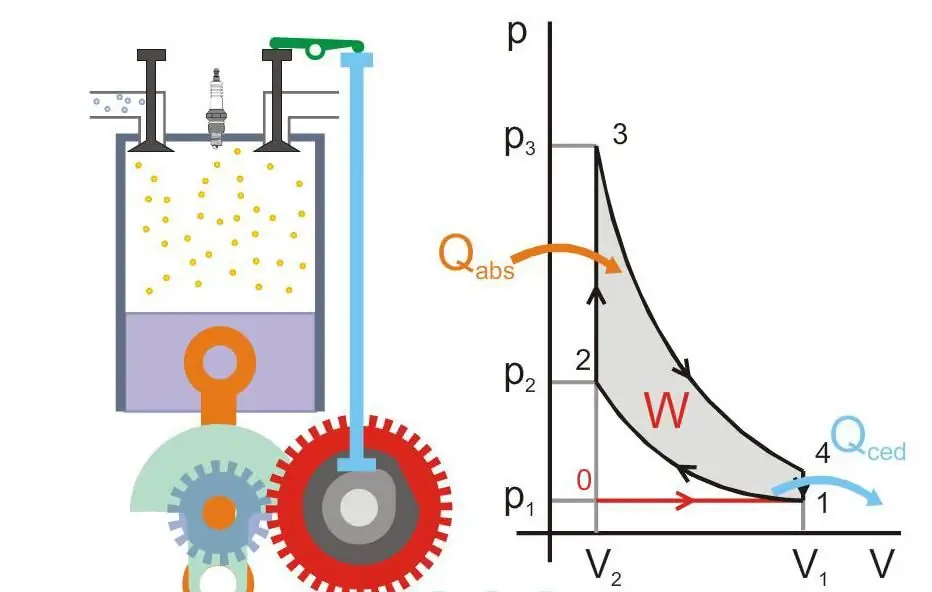
Zero absoluto e postulado de Nernst
Finalmente, passemos à consideração da terceira lei da termodinâmica. Também é chamado de postulado de Nernst (o nome do físico alemão que o formulou pela primeira vez no início do século XX). A lei diz: "O zero absoluto não pode ser alcançado com um número finito de processos." Ou seja, é impossível de alguma forma "congelar" completamente as moléculas e os átomos de uma substância. A razão para isso é a constante troca de calor existente com o meio ambiente.

Uma conclusão útil tirada da terceira lei da termodinâmica é que a entropia diminui à medida que nos aproximamos do zero absoluto. Isso significa que o sistema tende a se organizar. Este fato podeuse, por exemplo, para transferir paraímãs para um estado ferromagnético quando resfriado.
É interessante notar que a temperatura mais baixa que foi alcançada até agora é 5·10−10 K (2003, laboratório do MIT, EUA).






