O método condutométrico de análise é a medição da condutividade eletrolítica para monitorar o progresso de uma reação química. Esta ciência é amplamente aplicada em química analítica, onde a titulação é um método padrão de operação. O que é condutometria? Na prática comum em química analítica, o termo é usado como sinônimo de titulação, enquanto também é usado para descrever aplicações de não titulação. Qual é a vantagem de usar este método de análise? É frequentemente usado para determinar a condutividade geral de uma solução ou para analisar o ponto final de uma titulação envolvendo íons.
Histórico
Medidas condutivas começaram no século 18, quando Andreas Baumgartner notou que as águas salgadas e minerais de Bad Gastein emA Áustria conduz eletricidade. Assim, o uso desse método para determinar a pureza da água, que é frequentemente usado hoje para testar a eficácia dos sistemas de purificação de água, começou em 1776. Assim começou a história do método condutométrico de análise.
Friedrich Kohlrausch continuou o desenvolvimento desta ciência na década de 1860, quando aplicou corrente alternada à água, ácidos e outras soluções. Por volta dessa época, Willis Whitney, que estudava as interações dos complexos de ácido sulfúrico e sulfato de cromo, encontrou o primeiro ponto final condutométrico. Esses achados culminaram na titulação potenciométrica e no primeiro instrumento para análise volumétrica de Robert Behrend em 1883 na titulação de cloreto e brometo HgNO3. Assim, o método condutométrico moderno de análise é baseado em Behrend.
Este desenvolvimento permitiu testar a solubilidade de sais e a concentração de íons de hidrogênio, bem como titulações ácido-base e redox. O método condutométrico de análise foi aprimorado com o desenvolvimento do eletrodo de vidro, iniciado em 1909.
Titulação
Titulação condutométrica é uma medida na qual a condutividade eletrolítica de uma mistura de reação é monitorada continuamente pela adição de um reagente. O ponto de equivalência é o ponto em que a condutividade muda repentinamente. Um aumento ou diminuição notável na condutividade está associado a uma mudança na concentração dos dois íons mais altamente condutores, íons hidrogênio e hidróxido. Este métodopode ser usado para titular soluções coloridas ou suspensão homogênea (por exemplo, suspensão de polpa de madeira) que não pode ser usada com indicadores convencionais.
Titulações ácido-base e redox são frequentemente realizadas, que usam indicadores comuns para determinar o ponto final, como laranja de metila, fenolftaleína para titulação ácido-base e soluções de amido para um processo redox do tipo iodométrico. No entanto, as medições de condutividade elétrica também podem ser usadas como uma ferramenta para determinar o ponto final, por exemplo, ao observar uma solução de HCl com a base forte NaOH.
Neutralização de prótons
À medida que a titulação progride, os prótons são neutralizados para formar NaOH formando água. Para cada quantidade de NaOH adicionada, um número equivalente de íons de hidrogênio é removido. Com efeito, o cátion H+ móvel é substituído pelo íon Na+ menos móvel, e a condutividade da solução titulada, bem como a condutividade celular medida, diminui. Isso continua até que um ponto de equivalência seja alcançado no qual uma solução de cloreto de sódio NaCl possa ser obtida. Se mais base for adicionada, há um aumento à medida que mais íons Na+ e OH- são adicionados e a reação de neutralização não remove mais uma quantidade apreciável de H+.

Consequentemente, quando um ácido forte é titulado com uma base forte, a condutividade tem um mínimo no ponto de equivalência. Este mínimopode ser usado em vez de um corante indicador para determinar o ponto final de uma titulação. A curva de titulação é um gráfico de valores medidos de condutividade ou condutividade em função do volume de solução de NaOH adicionada. A curva de titulação pode ser usada para determinar graficamente o ponto de equivalência. O método condutométrico de análise (e seu uso) é extremamente relevante na química moderna.
Reação
Para uma reação entre um ácido fraco-base fraca, a condutividade elétrica primeiro diminui um pouco, uma vez que poucos íons H+ disponíveis são usados. Então a condutividade aumenta ligeiramente até o volume do ponto de equivalência devido à contribuição do cátion salino e do ânion (esta contribuição no caso de uma base ácida forte é desprezível e não é considerada lá)., a condutividade aumenta rapidamente devido a um excesso de íons OH.
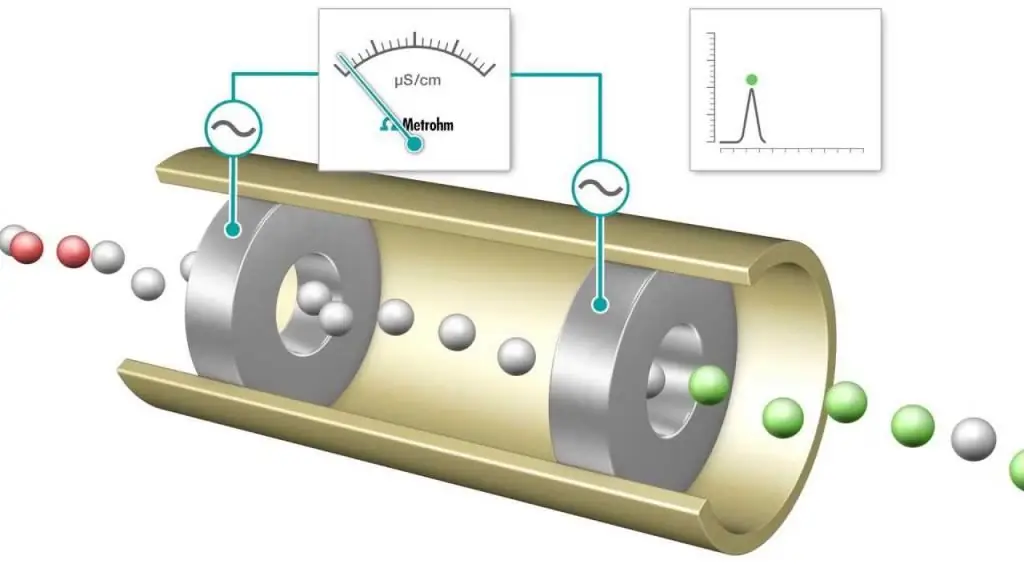
Os detectores de condutividade (método de análise condutométrico) também são usados para medir as concentrações de eletrólitos em soluções aquosas. A concentração molar do analito que cria a condutividade da solução pode ser obtida a partir da resistência elétrica medida da solução.
Método condutométrico de análise: princípio e fórmulas
(2.4.13) C=Constcell1Λm1Res, onde Constcell é um valor constante dependendo da célula de medição, Res é a resistência elétrica medida pelo dispositivo (de acordo com a lei de Ohm Res=I / V, e com uma constante tensão V medição I intensidade permite calcular Res), e Λm é o equivalentecondutividade para partículas iônicas. Embora para fins práticos Λm possa ser considerado constante, depende da concentração de acordo com a lei de Kohlrausch:
(2.4.14)=Хт Λm0-ΘC, onde Θ é uma constante e Λm0 é a condutividade molar limitante característica de cada íon. A condutividade molar, por sua vez, depende da temperatura.
Escrito
O desenvolvimento do método condutométrico de análise de medição levou os cientistas a novas descobertas. Os cientistas determinaram a razão crítica de supersaturação, Scrit, usando condutometria em um sistema de precipitação de AgCl homogêneo em excesso de íons Ag+, usando hidrólise de cloreto de alquila como fonte de íons CI.” Eles encontraram Scrit=1,51, 1,73 e 1,85 a 15, 25 e 35°C respectivamente, onde S=([Ag+][Cl-]/Ksp) 1/2 por sua definição. Se esta definição do fator de supersaturação for convertida para a nossa (S=[Ag+][Cl-] / Ksp), os resultados são 2,28, 2,99 e 3,42, respectivamente, em boa concordância com os resultados do presente estudo. No entanto, a dependência da temperatura do Scrit é oposta à descrita no presente estudo. Embora a razão para esta contradição não seja clara, a diminuição de Scrit com o aumento da temperatura pode ser bastante razoável, uma vez que a taxa de nucleação muda drasticamente com uma pequena mudança em ΔGm/ kT e, portanto, ΔGm/ kT, que é proporcional a T − 3 (lnSm) 2 de acordo com a fórmula (1.4.12) é considerado quase constante com a mudança de temperatura no sistema dado. Aliás, a definição de S deve ser [Ag +] [Cl -] / Ksp, pois a razão de supersaturação em termos deA concentração de monômero [AgCl] é inicialmente dada como S=[AgCl] / [AgCl] (∞)=[Ag +] [Cl -] / Ksp.
Tanaka e Iwasaki
A história do método condutométrico de análise foi continuada por dois icônicos cientistas japoneses. Tanaka e Iwasaki estudaram o processo de nucleação de partículas de AgCl e AgBr usando o método de fluxo interrompido em combinação com um espectrofotômetro multicanal, que é útil para estudar um processo rápido da ordem de mseg. Eles descobriram que algum complexo específico de haleto de prata AgXm (m-1), com uma banda de absorção de UV bastante estreita, foi formado instantaneamente quando uma solução de AgC104 da ordem de 10-4 mol dm-3 foi misturada com um KX (X=Cl ou Br) solução da ordem de 10-2 a 10-1 mol dm-3 seguido de seu rápido decaimento de cerca de 10 ms com a formação de um produto intermediário com uma ampla absorção de UV e uma mudança muito mais lenta no espectro do produto intermediário. Eles interpretaram o intermediário como núcleos monodispersos (AgX) n consistindo de n moléculas e determinaram n a partir da razão aparente -dC/dt α Cn em t=0 para várias concentrações iniciais do precursor C AgXm (m-1) - (n=7 -10 para AgCl, n=3-4 para AgBr).

No entanto, como o precursor AgXm (m − 1) decai de maneira não estacionária, a teoria da nucleação quase estacionária não se aplica a este processo e, portanto, o valor resultante de n não corresponde ao nvalor dos núcleos críticos. Se o produto intermediário contiver núcleos monodispersos n,formado pelo complexo monomérico, a razão -dC/dtαC pode não ser mantida. A menos que assumamos que clusters menores que n-mers estejam em equilíbrio, ki − 1, ici − 1c1=ki, i − 1ci, uns com os outros em uma reação sequencial c1 → c2 → c3 →… → cn − 1 → cn., e apenas o último passo cn − 1 → cn é irreversível; ou seja, c1⇌c2⇌c3⇌… ⇌cn − 1 → cn.
Além disso, deve-se supor que as concentrações de clusters de 2 a n-1 têm concentrações de equilíbrio desprezíveis. No entanto, parece não haver base para justificar essas suposições. Por outro lado, tentamos calcular os raios dos núcleos críticos e os coeficientes de supersaturação S no final do processo rápido, usando γ=101 mJ m − 2 para AgCl19 cúbico e γ=109 mJ m − 2 para AgBr20 cúbico, assumindo que os valores de n, 7-10 para AgCl19 e 3-4 para AgBr20, são equivalentes ao tamanho de núcleos monodispersos, n. O método condutométrico de análise, cujas revisões vão da simples aprovação à admiração, deu um novo nascimento à química como ciência.
Como resultado, os cientistas descobriram a seguinte fórmula: r=0,451 nm e S=105 para AgCl com n=9; r=0,358 nm e S=1230 para AgBr com n=4. Uma vez que seus sistemas são comparáveis aos de Davis e Jones, que obtiveram uma supersaturação crítica de AgCl de cerca de 1,7-2,0 a 25 °C. Usando condutometria de mistura direta em volumes iguais de soluções aquosas diluídas de AgNO3 e KCl, valores de S extremamente altos podem não refletir os fatores de supersaturação reais.em equilíbrio com núcleos intermediários.
absorção UV
Parece mais razoável atribuir um intermediário com ampla absorção de UV a núcleos muito maiores que a média com uma ampla distribuição de tamanhos gerada por uma reação sequencial não estacionária. A subsequente mudança lenta dos núcleos intermediários parece estar relacionada à sua maturação em Ostwald.

No contexto acima, o químico americano Nielsen também derivou um nsemelhante em torno de 12 e um S correspondente maior que 103 para a nucleação de partículas de sulfato de bário a partir de medições de turbidez em função da supersaturação, usando n=dlogJ / dlogC em uma teoria do tipo Becher-Dering para a fórmula. (1.3.37), mas dando (n+ 1) em vez de n. Como as soluções de íons de bário e íons de sulfato foram misturadas diretamente neste experimento, a nucleação transiente rápida deveria ter terminado imediatamente após a mistura, e o que foi medido poderia ser a taxa de maturação de Ostwald subsequente lenta e/ou fusão dos núcleos gerados. Aparentemente, esta é a razão para o valor excessivamente pequeno de n e a supersaturação extremamente alta. Portanto, devemos novamente notar que algum reservatório de espécies monoméricas que as libera em resposta ao seu consumo é sempre necessário para alcançar a nucleação quase estacionária em um sistema fechado. Todas as teorias clássicas de nucleação, incluindo a teoria de Becher-Döring, assumem implicitamente tal condição. Definição de condutométricométodo de análise foi dado nas seções do artigo acima.
Outros cientistas investigaram o processo de nucleação transitória de haleto de prata por radiólise pulsada de água contendo haleto de metileno e íons de prata, durante o qual o haleto de metileno é decomposto para liberar íons haleto por elétrons hidratados gerados por radiação pulsada na faixa de 4 ns a 3 µs. Os espectros dos produtos foram registrados usando um fotomultiplicador e uma câmera de raia e os precursores monoméricos de haleto de prata foram formados ao longo de um tempo da ordem de microssegundos, seguido por um processo de nucleação semelhante ao observado por Tanaka e Iwasaki. Seus resultados mostram claramente que o processo de nucleação de haletos de prata por mistura direta dos reagentes consiste em duas etapas elementares; ou seja, a formação de um precursor monomérico da ordem de μs e a subsequente transição para núcleos da ordem de 10 ms. Deve-se notar que o tamanho médio dos núcleos é de cerca de 10 nm.
Saturação
Em relação aos coeficientes de supersaturação para a nucleação de partículas de AgCl em sistemas abertos em que altas concentrações de reagentes como AgNO3 e KCl são continuamente introduzidas na solução de gelatina ao longo da precipitação, Strong e Wey31 relataram 1,029 (80°C) - 1,260 (40°C) e Leubner32 relataram 1,024 a 60°C como estimado a partir da medição da taxa de crescimento de partículas de sementes de AgCl em supersaturação crítica. Esta é a essência do método condutométrico de análise quantitativa.
Por outro lado, para sistemas abertos de partículas de AgBr, algunsvalores estimados do coeficiente de supersaturação crítico, Scrit: Scrit∼- 1,5 a 70 °C de acordo com Wey e Strong33 a partir da taxa de crescimento máxima dependente do tamanho determinada encontrando o limiar de renucleação em diferentes taxas de adição de uma solução de AgNO3 a um KBr solução na presença de partículas de sementes pelos jatos duplos; Scrit=1,2-1,5 a 25°C de acordo com Jagannathan e Wey34 como o fator de supersaturação máximo determinado a partir da equação de Gibbs-Thomson com seus dados sobre o tamanho médio mínimo dos núcleos observados por microscopia eletrônica durante a etapa de nucleação da precipitação de AgBr de dois jatos. Isso é muito eficaz ao aplicar o método de quantificação condutométrica.

Ao calcular esses valores de Scrit, eles tomaram γ=140 mJ m − 2. Como a nucleação em sistemas abertos corresponde ao processo de sobrevivência de núcleos nascentes criados em uma zona local de supersaturação extremamente alta perto das saídas dos reagentes, crítico a supersaturação corresponde à concentração do soluto em equilíbrio com núcleos de tamanho máximo, se usarmos os dados de Sugimoto35 sobre o raio máximo dos núcleos de AgBr em sistemas abertos (0,3 8,3 nm) com γ teórico para AgBr cúbico (=109 mJ m − 2) 3, então o fator crítico de supersaturação, Scrit, é calculado como seria 1,36 a 25°C (se γ for assumido como 140 mJ/m2, então Scrit=1,48).
Conseqüentemente, em qualquer caso, supersaturações críticas emsistemas abertos de partículas de haleto de prata estão tipicamente bem abaixo das supersaturações máximas (provavelmente próximas a supersaturações críticas) em sistemas fechados. Isso ocorre porque o raio médio dos núcleos gerados na zona local de um sistema aberto é muito maior que rm em um sistema fechado, provavelmente devido à fusão instantânea de núcleos primários altamente concentrados na zona local de um sistema aberto com alta concentração local de eletrólitos.
Aplicativo
O uso do método de titulação condutométrica para registro contínuo durante processos enzimáticos tem sido amplamente estudado e analisado. Quase todos os métodos analíticos eletroquímicos são baseados em reações eletroquímicas (potenciometria, voltametria, amperometria, coulometria).
O método condutométrico de análise é um método no qual não há reações eletroquímicas nos eletrodos ou há reações secundárias que podem ser desprezadas. Portanto, neste método, a propriedade mais importante da solução eletrolítica na camada limite é sua condutividade elétrica, que varia de acordo com uma gama bastante ampla de reações biológicas.
Benefícios
Os biossensores condutométricos também apresentam algumas vantagens em relação a outros tipos de transdutores. Primeiro, eles podem ser feitos usando tecnologia padrão de filme fino de baixo custo. Isso, juntamente com o uso de um método otimizado de imobilização de material biológico, leva a uma redução significativa tanto no custo primário dos dispositivos quantocusto total da análise. Para microbiosensores integrados, é fácil executar o modo de medição diferencial, que compensa as influências externas e melhora muito a precisão da medição.
Os dados mostram claramente o grande potencial dos biossensores condutométricos. No entanto, esta ainda é uma tendência relativamente nova em biossensores, portanto, o desenvolvimento de dispositivos comerciais tem um futuro promissor.
Novos métodos
Alguns cientistas descreveram um método geral para medir pKa por condutância. Este método foi amplamente utilizado até cerca de 1932 (antes dos métodos de medição de pH serem usados). O método condutométrico é extremamente sensível à temperatura e não pode ser usado para medir valores de pKa sobrepostos. Uma possível vantagem para amostras sem cromóforo é que ele pode ser usado em soluções muito diluídas, até 2,8 × 10-5 M. Nos últimos anos, a condutometria 87 tem sido usada para medir o pKa da lidocaína, embora o resultado obtido tenha sido de 0,7 por unidade abaixo do valor de pH geralmente aceito.

Albert e Sergeant também descreveram um método para determinar pKa a partir de medições de solubilidade. Como mencionado acima, a solubilidade depende do pKa, portanto, se a solubilidade for medida em vários valores de pH em uma curva, o pKa pode ser determinado. Peck e Benet descreveram um método geral para estimar os valores de pKa para substâncias monopróticas, dipróticas e anfotéricas, dado um conjunto de medições de solubilidade e pH. Hansen e Hafliger obtiveram o pKa da amostra, querapidamente se decompõe por hidrólise a partir de suas taxas de dissolução iniciais em função do pH em um dispositivo de disco rotativo. O resultado concorda bem com o resultado de pH/UV, mas a decomposição dificulta o último método. Esta é, em geral, uma descrição do método condutométrico de análise.






