A capacidade calorífica de um gás é a quantidade de energia que um corpo absorve quando é aquecido em um grau. Vamos analisar as principais características desta grandeza física.

Definições
O calor específico de um gás é a unidade de massa de uma determinada substância. Suas unidades de medida são J/(kg·K). A quantidade de calor que é absorvida pelo corpo no processo de mudança de seu estado de agregação está associada não apenas ao estado inicial e final, mas também ao método de transição.

Departamento
A capacidade calorífica dos gases é dividida pelo valor determinado a volume constante (Cv), pressão constante (Cр).
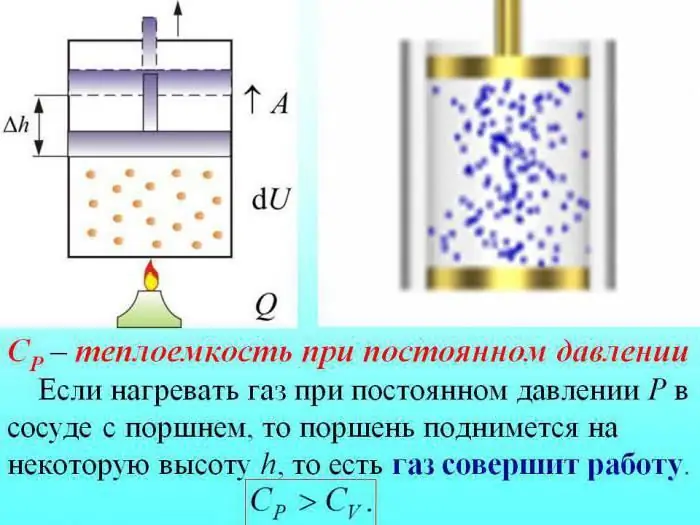
No caso de aquecimento sem alterar a pressão, algum calor é gasto para produzir o trabalho de expansão do gás, e parte da energia é gasta para aumentar a energia interna.
A capacidade calorífica dos gases a pressão constante é determinada pela quantidade de calor que é gasta no aumento da energia interna.
Estado do gás: características, descrição
A capacidade calorífica de um gás ideal é determinada levando em consideração o fato de que Сp-Сv=R. A última quantidade é chamada de constante universal do gás. Seu valor corresponde a 8,314 J/(mol K).
Ao realizar cálculos teóricos de capacidade calorífica, por exemplo, descrevendo a relação com a temperatura, não basta usar apenas métodos termodinâmicos, é importante se armar com elementos da física estática.
A capacidade calorífica dos gases envolve o cálculo do valor médio da energia do movimento de translação de algumas moléculas. Tal movimento se resume ao movimento de rotação e translação da molécula, bem como das vibrações internas dos átomos.
Na física estática, há informações de que para cada grau de liberdade de movimento rotacional e translacional, existe uma quantidade para um gás que é igual à metade da constante universal do gás.

Fatos interessantes
Assume-se que uma partícula de um gás monoatômico tem três graus de liberdade translacionais, de modo que o calor específico de um gás tem três graus de liberdade translacionais, dois rotacionais e um vibracional. A lei de sua distribuição uniforme leva a igualar o calor específico a um volume constante a R.
Durante os experimentos, verificou-se que a capacidade calorífica de um gás diatômico corresponde ao valor R. Tal discrepância entre a teoria e a prática é explicada pelo fato de que a capacidade calorífica de um gás ideal está associada ao quantum efeitos, portanto, ao fazer cálculos, é importante usar estatísticas baseadas emmecânica.
Baseado nos fundamentos da mecânica quântica, qualquer sistema de partículas que oscilam ou giram, incluindo moléculas de gás, tem apenas alguns valores discretos de energia.
Se a energia do movimento térmico no sistema não for suficiente para excitar oscilações de uma certa frequência, tais movimentos não contribuem para a capacidade calorífica total do sistema.
Como resultado, um determinado grau de liberdade fica "congelado", sendo impossível aplicar a lei da equipartição a ele.
A capacidade calorífica dos gases é uma característica importante do estado do qual depende o funcionamento de todo o sistema termodinâmico.
A temperatura na qual a lei da equipartição pode ser aplicada ao grau de liberdade vibracional ou rotacional é caracterizada pela teoria quântica, conecta a constante de Planck com a constante de Boltzmann.

Gases diatômicos
As lacunas entre os níveis de energia rotacional de tais gases são um pequeno número de graus. A exceção é o hidrogênio, no qual o valor da temperatura é determinado por centenas de graus.
É por isso que a capacidade calorífica de um gás a pressão constante é difícil de descrever pela lei da distribuição uniforme. Na estatística quântica, ao determinar a capacidade calorífica, leva-se em consideração que sua parte vibracional, no caso de diminuição da temperatura, diminui rapidamente e chega a zero.
Esse fenômeno explica o fato de que à temperatura ambiente praticamente não há parte vibracional da capacidade calorífica, porgás diatômico, corresponde à constante R.
A capacidade calorífica de um gás a volume constante no caso de indicadores de baixa temperatura é determinada usando estatísticas quânticas. Existe o princípio de Nernst, que é chamado de terceira lei da termodinâmica. Com base em sua formulação, a capacidade calorífica molar de um gás diminuirá com a diminuição da temperatura, tendendo a zero.

Características dos sólidos
Se a capacidade calorífica de uma mistura de gases pode ser explicada usando estatísticas quânticas, então, para um estado sólido de agregação, o movimento térmico é caracterizado por pequenas flutuações de partículas próximas à posição de equilíbrio.
Cada átomo possui três graus de liberdade vibracional, portanto, de acordo com a lei da equipartição, a capacidade calorífica molar de um sólido pode ser calculada como 3nR, sendo n o número de átomos em uma molécula.
Na prática, este número é o limite para o qual a capacidade calorífica de um corpo sólido tende a altas temperaturas.
O máximo pode ser obtido em temperaturas normais para alguns elementos, incluindo metais. Para n=1, a lei de Dulong e Petit é cumprida, mas para substâncias complexas é bastante difícil atingir tal limite. Como o limite não pode ser obtido na realidade, ocorre a decomposição ou fusão do sólido.
História da teoria quântica
Os fundadores da teoria quântica são Einstein e Debye no início do século XX. Baseia-se na quantização de movimentos oscilatórios de átomos em um determinadocristal. No caso de indicadores de baixa temperatura, a capacidade calorífica de um corpo sólido acaba sendo diretamente proporcional ao valor absoluto tomado ao cubo. Essa relação tem sido chamada de lei de Debye. Como critério que permite distinguir entre indicadores de baixa e alta temperatura, toma-se sua comparação com a temperatura de Debye.
Esse valor é determinado pelo espectro de vibrações de um átomo no corpo, portanto, depende seriamente das características de sua estrutura cristalina.
QD é um valor que tem várias centenas de K, mas, por exemplo, é muito maior em diamante.
Os elétrons de condução contribuem significativamente para a capacidade calorífica dos metais. Para calculá-lo, são utilizadas as estatísticas quânticas de Fermi. A condutividade eletrônica para átomos de metal é diretamente proporcional à temperatura absoluta. Por ser um valor insignificante, é levado em consideração apenas em temperaturas tendendo ao zero absoluto.
Métodos para determinar a capacidade calorífica
O principal método experimental é a calorimetria. Para realizar um cálculo teórico da capacidade calorífica, é utilizada a termodinâmica estatística. É válido para um gás ideal, assim como para corpos cristalinos, é realizado com base em dados experimentais sobre a estrutura da matéria.
Métodos empíricos para calcular a capacidade calorífica de um gás ideal são baseados na ideia da estrutura química, a contribuição de grupos individuais de átomos para Ср.
Para líquidos, também são usados métodos baseados no uso de termodinâmicosciclos que permitem passar da capacidade calorífica de um gás ideal para um líquido através da derivada da temperatura da entalpia do processo de evaporação.
No caso de uma solução, o cálculo da capacidade calorífica como uma função aditiva não é permitido, pois o valor excedente da capacidade calorífica da solução é basicamente significativo.
Para avaliá-lo, precisamos da teoria estatística-molecular das soluções. O mais difícil é a identificação da capacidade calorífica de sistemas heterogêneos na análise termodinâmica.

Conclusão
O estudo da capacidade calorífica permite calcular o balanço energético dos processos que ocorrem em reatores químicos, bem como em outros aparelhos de produção química. Além disso, este valor é necessário para a seleção de tipos ideais de refrigerantes.
Atualmente, a determinação experimental da capacidade calorífica de substâncias para vários intervalos de temperatura - de valores baixos a valores altos - é a principal opção para determinar as características termodinâmicas de uma substância. Ao calcular a entropia e a entalpia de uma substância, são usadas integrais de capacidade calorífica. As informações sobre a capacidade calorífica dos reagentes químicos em uma determinada faixa de temperatura permitem calcular o efeito térmico do processo. As informações sobre a capacidade calorífica das soluções permitem calcular seus parâmetros termodinâmicos em quaisquer valores de temperatura dentro do intervalo analisado.
Por exemplo, um líquido é caracterizado pelo gasto de parte do calor para alterar o valor da energia potencialmoléculas reagentes. Esse valor é chamado de capacidade calorífica de "configuração", usado para descrever soluções.
É difícil realizar cálculos matemáticos completos sem levar em conta as características termodinâmicas de uma substância, seu estado de agregação. É por isso que para líquidos, gases, sólidos, é usada uma característica como capacidade calorífica específica, que permite caracterizar os parâmetros de energia de uma substância.






