A teoria cinética molecular permite, analisando o comportamento microscópico do sistema e utilizando os métodos da mecânica estatística, obter importantes características macroscópicas do sistema termodinâmico. Uma das características microscópicas, que está relacionada com a temperatura do sistema, é a velocidade quadrática média das moléculas do gás. Damos a fórmula para isso e a consideramos no artigo.
Gás Ideal
Observamos imediatamente que a fórmula para a velocidade média quadrática das moléculas de gás será dada especificamente para um gás ideal. Sob ele, na física, é considerado um sistema de muitas partículas no qual as partículas (átomos, moléculas) não interagem umas com as outras (sua energia cinética excede a energia potencial de interação em várias ordens de magnitude) e não têm dimensões, isto é, eles são pontos com uma massa finita (a distância entre partículas várias ordens de grandeza maior que seu tamanho.linear).
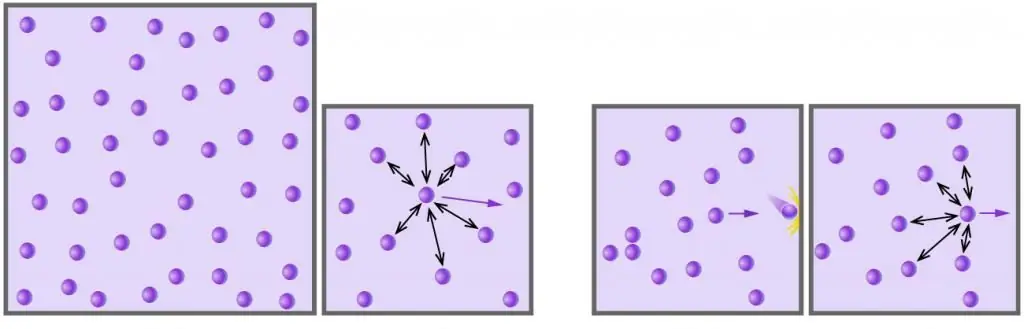
Qualquer gás que consiste em moléculas ou átomos quimicamente neutros, e que está sob baixa pressão e tem alta temperatura, pode ser considerado ideal. Por exemplo, o ar é um gás ideal, mas o vapor de água não é mais assim (fortes ligações de hidrogênio agem entre as moléculas de água).
Teoria Cinética Molecular (MKT)

Estudando um gás ideal no âmbito do MKT, deve-se atentar para dois processos importantes:
- O gás cria pressão transferindo para as paredes do recipiente que o contém, o momento quando moléculas e átomos colidem com eles. Essas colisões são perfeitamente elásticas.
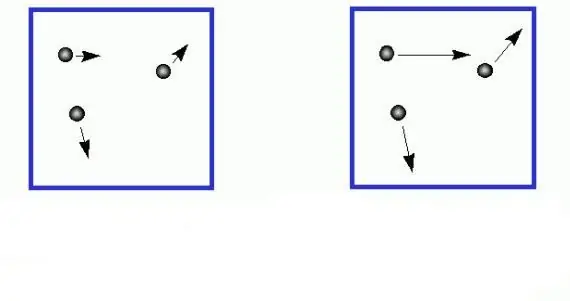
- Moléculas e átomos de gás se movem aleatoriamente em todas as direções com diferentes velocidades, cuja distribuição obedece à estatística de Maxwell-Boltzmann. A probabilidade de colisão entre as partículas é extremamente baixa, devido ao seu tamanho desprezível e às grandes distâncias entre elas.
Apesar do fato de que as velocidades individuais das partículas de gás são muito diferentes umas das outras, o valor médio deste valor permanece constante ao longo do tempo se não houver influências externas no sistema. A fórmula para a velocidade quadrática média das moléculas de gás pode ser obtida considerando a relação entre energia cinética e temperatura. Trataremos dessa questão no próximo parágrafo do artigo.
Derivação da fórmula para a velocidade média quadrática de moléculas de gás ideal
Todo estudante sabe do curso geral de física que a energia cinética do movimento de translação de um corpo de massa m é calculada da seguinte forma:
Ek=mv2/2
Onde v é a velocidade linear. Por outro lado, a energia cinética de uma partícula também pode ser determinada em termos da temperatura absoluta T, usando o fator de conversão kB(constante de Boltzmann). Como nosso espaço é tridimensional, Ek é calculado da seguinte forma:
Ek=3/2kBT.
Equivalente a ambas as igualdades e expressando v delas, obtemos a fórmula para a velocidade média de um gás quadrático ideal:
mv2/2=3/2kBT=>
v=√(3kBT/m).
Nesta fórmula, m - é a massa da partícula de gás. Seu valor é inconveniente para uso em cálculos práticos, pois é pequeno (≈ 10-27kg). Para evitar esse inconveniente, lembremos a constante universal do gás R e a massa molar M. A constante R com kB está relacionada pela igualdade:
kB=R/NA.
O valor de M é definido da seguinte forma:
M=mNA.
Considerando ambas as igualdades, obtemos a seguinte expressão para a velocidade quadrática média das moléculas:
v=√(3RT/M).
Assim, a velocidade quadrada média das partículas de gás é diretamente proporcional à raiz quadrada da temperatura absoluta e inversamente proporcional à raiz quadrada da massa molar.
Exemplo de resolução de problemas
Todo mundo sabe que o ar que respiramos é 99% nitrogênio e oxigênio. É necessário determinar as diferenças nas velocidades médias das moléculas N2 e O2 a uma temperatura de 15 o C.

Este problema será resolvido sequencialmente. Primeiro, traduzimos a temperatura em unidades absolutas, temos:
T=273, 15 + 15=288, 15 K.
Agora escreva as massas molares para cada molécula em consideração:
MN2=0,028 kg/mol;
MO2=0,032 kg/mol.
Como os valores das massas molares diferem ligeiramente, suas velocidades médias na mesma temperatura também devem ser próximas. Usando a fórmula para v, obtemos os seguintes valores para as moléculas de nitrogênio e oxigênio:
v (N2)=√(38, 314288, 15/0, 028)=506,6 m/s;
v (O2)=√(38, 314288, 15/0, 032)=473,9 m/s.
Como as moléculas de nitrogênio são ligeiramente mais leves que as moléculas de oxigênio, elas se movem mais rápido. A diferença de velocidade média é:
v (N2) - v (O2)=506,6 - 473,9=32,7 m/s.
O valor resultante é apenas 6,5% da velocidade média das moléculas de nitrogênio. Chamamos a atenção para as altas velocidades das moléculas nos gases, mesmo em baixas temperaturas.






